-

미 FDA, 렘데시비르 정식 사용 승인...‘첫 코로나19 치료제 탄생’
2020.10.23 19:04 -

WHO “렘데시비르 코로나 치료 효과 없어”...국내 환자 600여 명 투여
2020.10.16 20:27 -

중대본 “렘데시비르 투여 106명 중 4명 ‘이상반응’…효과 검토 중”
2020.08.04 17:01 -
식약처, 코로나19 치료제 ‘렘데시비르’ 품목 허가
2020.07.24 13:30 -
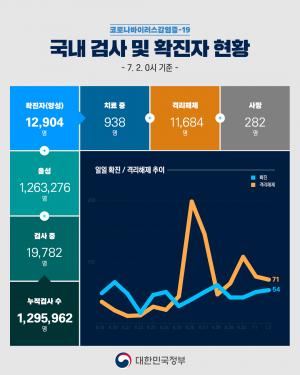
국내 코로나 중증 확진자 두 명에게 렘데시비르 투약
2020.07.02 18:37
