-

김강립 식약처 전 처장 청탁금지법 위반 혐의로 압수수색 진행
2023.08.28 17:50 -

의원급 의료기관 중심 비대면 진료 제도화로 '의료사각지대' 해소
2023.03.03 09:17 -

‘K-바이오·백신펀드’ 5000억원 조성
2022.07.28 11:34 -

‘국내개발 1호’ 코로나19 백신 중앙약심 통과
2022.06.27 15:32 -

식약처, 5∼11세용 코로나 백신 품목허가…예방효과 90.7%
2022.02.23 14:40 -

식약처, 국내 제조 ‘노바백스사’ 코로나19 백신 품목허가
2022.01.13 11:16 -

코로나19 치료제 및 백신개발 등에 총 5457억원 지원
2021.12.24 11:03 -

FDA, '먹는 알약' 코로나 치료제 첫 승인
2021.12.23 14:22 -

화이자, FDA에 코로나 치료 알약 긴급승인 신청
2021.11.17 09:54 -
셀트리온 렉키로나 유럽승인 전 해결해야할 국내 위드코로나 과제 '산적'
2021.11.08 14:17 -

코로나19 먹는 치료제 곧 나오나…머크 FDA 긴급사용 신청
2021.10.12 11:04 -
접종완료자, 확진자와 밀접접촉해도 증상없으면 자가격리 면제
2021.09.24 15:11 -

국산 1호 코로나 백신 개발 속도…5년간 2.2조 투입
2021.08.06 11:23 -

국내 코로나19 백신 개발 5개사 임상 1상 완료
2021.06.08 17:27 -

화이자 백신 사용연령 확대 추진...“전국민 코로나19 면역체계 달성을 위해“
2021.05.07 16:23 -
식약처, AZ 코로나19 백신에 ‘혈전증’ 주의사항 추가
2021.04.28 16:33 -
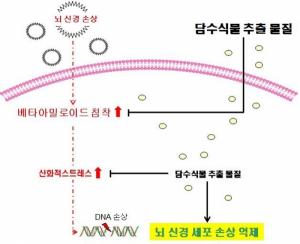
담수식물 활용해 치매 개선 건강기능식품 만든다
2021.04.22 15:01 -

불가리스에 코로나19 예방 효과 있다던 남양유업, “오해 일으켜 죄송합니다”
2021.04.16 14:42 -
“한 번만 맞으면 끝” 얀센 코로나19 백신, 국내 세 번째로 품목허가 승인
2021.04.07 16:06 -

AZ, 만 65세 이상 고령층도 이제 맞을 수 있다
2021.03.11 16:05
