-

의원급 의료기관 중심 비대면 진료 제도화로 '의료사각지대' 해소
2023.03.03 09:17 -

‘감염병·희귀질환 치료’ 첨단바이오의약품, 신속 허가한다
2020.09.08 19:11 -

식약처, 의료제품 허가·심사 체계 개편..."전문성 강화·심사기간 단축에 기여"
2020.08.19 18:44 -

식약처, 코오롱생명과학 ‘인보사’ 허가취소·형사고발 조치
2019.05.28 14:28 -
바이오신약 인보사, 제2의 황우석 사건되나
2019.04.17 19:11 -
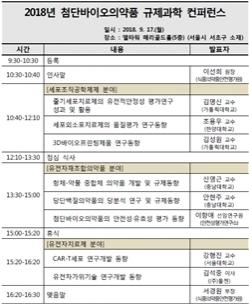
식약처, 17일 ‘2018년 첨단바이오의약품 규제과학 컨퍼런스’ 개최
2018.09.14 13:10
