-

내년 백신 9000만 회분 구매…1분기 내 대다수 3차 접종 마무리
2021.12.31 11:14 -

코로나19 치료제 및 백신개발 등에 총 5457억원 지원
2021.12.24 11:03 -

식약처, 화이자 먹는 치료체 긴급사용 검토 착수
2021.12.22 14:41 -

국산 1호 코로나 백신 개발 속도…5년간 2.2조 투입
2021.08.06 11:23 -
종근당 등 국내 제약사, 코로나19 치료제 허가 경쟁 불붙나?
2021.02.09 11:05 -
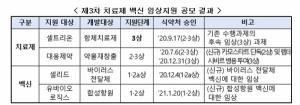
정부, ‘코로나19 종식 희망’ 4개 기업에 임상지원 결정
2021.01.26 18:56 -

셀트리온 검증 자문 결과, “임상 3상 전제로 허가 권고”
2021.01.18 19:22 -

셀트리온 코로나19 치료제 검증 결과, 18일 공개된다
2021.01.14 18:47 -

노바백스 백신도 긍정 신호...“전 국민 접종 물량 확보했다”
2021.01.12 19:01 -

“구충제 이버멕틴, 코로나19 치사율 최대 80% 낮춰”
2021.01.05 18:10 -

코로나19 백신 내년 하반기부터 접종 예정...“신중히 결정할 것”
2020.11.19 19:01 -
“코로나19 한 줄기 빛을 찾아서”...국내 치료제·백신 임상 21건
2020.11.10 19:11 -

안과질환 건강보험 적용...“눈 아픈 환자 부담 대폭 줄어든다”
2020.10.30 18:42 -

미 FDA, 렘데시비르 정식 사용 승인...‘첫 코로나19 치료제 탄생’
2020.10.23 19:04 -

WHO “렘데시비르 코로나 치료 효과 없어”...국내 환자 600여 명 투여
2020.10.16 20:27 -

‘감염병·희귀질환 치료’ 첨단바이오의약품, 신속 허가한다
2020.09.08 19:11 -

정부, 3차추경 1936억 코로나 국내 치료제 개발 투입
2020.07.09 17:45 -

정부, 코로나19 백신 생산 적극 지원 나선다
2020.06.24 10:44 -
유명희 통상교섭본부장, 코로나19 치료제 및 신속 진단키트 개발기업 격려
2020.03.21 11:25 -

독일 바이엘 '클로로퀸' 코로나19 구원투수 될까?
2020.03.20 16:48
